醫療器械不良事件監測管理辦法(征求意見稿)
格式:pdf
大小:8KB
頁數:3P
人氣 :91
4.7
1 醫療器械不良事件監測管理辦法(征求意見稿) 各省、自治區、直轄市食品藥品監督管理局(藥品監督管理局)、衛生廳(局): 為全面加強我國醫療器械上市后的監管, 建立和完善醫療器械不良事件監測體系, 國家食品藥 品監督管理局會同衛生部起草了《醫療器械不良事件監測管理辦法(征求意見稿)》,請提出修改 意見,必要時可召開座談會聽取省級藥品不良反應監測中心、醫療器械生產企業、經營企業、醫療 預防保健機構和有關專家的意見。修改意見請于 2004年 3月 1 日之前書面分別報送國家食品藥品 監督管理局醫療器械司和衛生部醫政司。 國家食品藥品監督管理局 衛生部辦公室廳 二○○四年一月六日 醫療器械不良事件監測管理辦法 (征求意見稿) 第一章 總則 第一條 為了加強對上市后醫療器械的監督管理, 確保醫療器械使用的安全有效,根據《醫療 器械監督管理條例》,制定本辦法。 第二條 國家食品藥品監督管理局主管全

河南省醫療器械不良事件監測和再評價管理辦法實施細則
格式:pdf
大小:81KB
頁數:15P
河南省醫療器械不良事件監測和再評價管理 辦法實施細則(試行) 第一章總則 第一條為加強上市醫療器械的安全監管,規范醫療器械不良事件監測 和再評價工作,保障公眾用械安全,根據《醫療器械監督管理條例》和《醫 療器械不良事件監測和再評價管理辦法(試行)》,結合我省實際,制定本 細則。 第二條本細則適用于河南省行政區域內的醫療器械生產企業、經營企業、 使用單位、醫療器械不良事件監測技術機構、食品藥品監督管理部門和其 他有關主管部門。 第三條鼓勵公民、法人和其他相關社會組織報告醫療器械不良事件。 第二章管理職責 第四條省食品藥品監督管理局主管全省醫療器械不良事件監測和再評 價工作,并履行以下主要職責: (一)會同省衛生廳制定全省醫療器械不良事件監測及管理規定,并監 督實施; (二)會同省衛生廳組織全省醫療器械不良事件監測的宣傳、教育、培 訓工作; (三)負責指導全省醫療器械不良事件

醫療器械不良事件報告工作程序
格式:pdf
大小:21KB
頁數:4P
文件名稱醫療器械不良事件報告工作程序 文件編號版本編制日期編制部門 批準審核編制受控狀態 版本號修改日期修改內容修定人 醫療器械不良事件報告工作程序 1目的 根據國食藥監械2008年第766號《醫療器械不良事件監測和再評價管理辦法(試行)》、 國食藥監械2011年425號《醫療器械不良事件工作指南(試行)》制訂,規定我公司醫療 器械可疑不良事件和不良事件的監測、報告程序和再評價要求。 2范圍 適用于公司所有在中國境內銷售的醫療器械產品的不良事件監測和再評價的控制。 3相關文件 醫療器械不良事件監測和再評價管理辦法(試行) 醫療器械不良事件工作指南(試行) 4術語 4.1不良事件:是指獲準上市的質量合格的醫療器械在正常使用情況下發生的,導致或者可 能導致人體傷害的各種有害事件。 4.2不良事件監測:對醫療器械不良事件的發現、報告、評價和控制的
編輯推薦下載

醫療器械監督檢查員管理辦法
格式:pdf
大小:12KB
頁數:9P
4.7
—2— 附件 醫療器械監督檢查員管理辦法 (征求意見稿) 第一章總則 第一條為加強醫療器械監督檢查員(以下簡稱檢查員) 的管理,做好醫療器械監督管理工作,依據《醫療器械監督 管理條例》等法規規章,制定本辦法。 第二條本辦法適用于依照醫療器械法規和相應質量管 理規范對醫療器械生產、經營或使用等環節開展檢查的相關 檢查員的管理。 第三條國家食品藥品監督管理總局(以下簡稱總局)對檢 查員實行分級管理,檢查員分為國家級、省級、地市級和區縣級。 第四條總局負責制定全國檢查員隊伍建設的總體規劃, 制定發布檢查員管理制度并指導全國檢查員管理工作。 省級及以下食品藥品監督管理部門分別負責本轄區內相 應檢查員隊伍的建設規劃和管理。 第五條總局組織編寫統一的培訓教材,建立統一的考試 題庫,統一組織開展師資培訓。 第六條檢查員隊伍實行單位審核、教育培訓、資格考試、 考察聘用和綜合考評的動態管理

醫療器械注冊管理辦法【最新】
格式:pdf
大小:40KB
頁數:14P
4.5
國家食品藥品監督管理總局令 第4號 《醫療器械注冊管理辦法》已于2014年6月27日經國家食品藥品監督管理 總局局務會議審議通過,現予公布,自2014年10月1日起施行。 局長張勇 2014年7月30日 醫療器械注冊管理辦法 第一章總則 第一條為規范醫療器械的注冊與備案管理,保證醫療器械的安全、有效, 根據《醫療器械監督管理條例》,制定本辦法。 第二條在中華人民共和國境內銷售、使用的醫療器械,應當按照本辦法的 規定申請注冊或者辦理備案。 第三條醫療器械注冊是食品藥品監督管理部門根據醫療器械注冊申請人 的申請,依照法定程序,對其擬上市醫療器械的安全性、有效性研究及其結果進 行系統評價,以決定是否同意其申請的過程。 醫療器械備案是醫療器械備案人向食品藥品監督管理部門提交備案資料,食 品藥品監督管理部門對提交的備案資料存檔備查。 第四條醫療器械注
醫療器械不良事件監測管理辦法熱門文檔

醫療器械召回管理辦法(征求意見稿)
格式:pdf
大小:34KB
頁數:8P
4.4
醫療器械召回管理辦法(征求意見稿) 第一章總則 第一條為了加強對醫療器械的監督管理,保障人體健康和生命安全,根據《醫療器械 監督管理條例》、《國務院關于加強食品等產品安全監督管理的特別規定》,制定本辦法。 在中華人民共和國境內銷售的醫療器械的召回及其監督管理,適用本辦法。 第二條本辦法所稱醫療器械召回,是指醫療器械生產企業按照規定的程序對其已上市 銷售的存在安全隱患的產品,按照規定的程序,采取警示、檢查、修理、重新標簽、修改說 明書、軟件升級、替換、收回、銷毀等方式消除其產品危害的行為。 第三條本辦法所稱安全隱患,是指由于研發、生產等原因使醫療器械在正常使用情況 下具有可能危及人體健康和生命安全的不合理危險。 第四條已上市銷售的醫療器械存在以下安全隱患的,應當召回: (一)因設計、制造上的缺陷已造成人體傷害的; (二)雖未造成人體傷害,但經檢測、試驗和論證,在特定條件

《醫療器械召回管理辦法(征求意見稿)》征求意見
格式:pdf
大小:54KB
頁數:9P
4.5
www.***.***免費法律咨詢3分鐘100%回復 上網找律師就到中顧法律網快速專業解決您的法律問題http://www.***.***/souask/ 文章來源:中顧法律網 《醫療器械召回管理辦法(征求意見稿)》征求意見 摘要:各有關單位: 為貫徹落實《國務院關于加強食品等產品安全監督管理的特別規定》,我局組織起草了《醫療器械召回 管理辦法(征求意見稿)》,現在我局網站予以公布,公開征求各有關方面的意見和建議。請務必將意見和建議 于2008年3月31日前反饋至國家食品藥品監督管理局政策法規司法規處。 國家食品藥品監督管理局政策法規司 二○○八年三月十八日 第一章總則 第一條為了加強對醫療器械的監督管理,保障人體健康和生命安全,根據《醫療器械監督管理條例》、《國 務院關于加強食品等產品安全監督管理的特別規定》,制定本辦法。 在中華人民共和國境內銷售的

醫療器械注冊管理辦法(征求意見稿)
格式:pdf
大小:95KB
頁數:29P
4.3
-3- 附件: 醫療器械注冊管理辦法 (征求意見稿) 第一章總則 第一條為規范醫療器械產品的注冊管理,保證醫療器械安 全有效,根據《醫療器械監督管理條例》,制定本辦法。 第二條在中國境內銷售、使用的醫療器械均應按本辦法的 規定申報注冊,未經注冊的醫療器械,不得銷售、使用。 第三條醫療器械注冊,是指依照法定程序,對擬上市銷售、 使用的醫療器械的安全性、有效性進行系統評價,做出是否同意 其銷售、使用的許可。 第四條國家對醫療器械注冊實行分類管理。 境內第一類醫療器械由設區市(食品)藥品監督管理局審查, 批準后發給注冊證書。 境內第二類醫療器械由省級(食品)藥品監督管理局審查, 批準后發給醫療器械注冊證書; 境內第三類醫療器械由國家(食品)藥品監督管理局審查, 批準后發給醫療器械注冊證書; 境外醫療器械由國家(食品)藥品監督管理局審查,批準后 發給醫療器械注冊證書。

北京市藥品監督管理局發布實施《北京市〈醫療器械不良事件監測和再評價管理辦法(試行)〉實施細則》
格式:pdf
大小:29KB
頁數:5P
4.7
北京市藥品監督管理局發布實施《北京市〈醫療器械不良事件監測和再評 價管理辦法(試行)〉實施細則》 發布時間:2011-06-22 北京市藥品監督局發布實施《北京市〈醫療器械 不良事件監測和再評價管理辦法(試行)〉實施細則》 為保障患者用械安全,依據《醫療器械監督管理條例》(國務院令第276 號)和《醫療器械不良事件監測和再評價管理辦法(試行)》(國食藥監械[2008]766 號),北京市藥品監督管理局結合本市醫療器械監管實際情況,經過近兩年的走 訪和調研,聯合北京市衛生局于近日發布了《北京市〈醫療器械不良事件監測和 再評價管理辦法(試行)〉實施細則》(以下簡稱《實施細則》)。 《實施細則》的發布旨在確立北京市醫療器械不良事件監測工作要求,明確 我市各部門職責分工,建立我市醫療器械不良事件報告、調查、評價、風險控制、 上市后醫療器械的再評價以及監測工作監督與管理的工作規范
醫療器械不良事件監測管理辦法精華文檔

醫療器械監督檢查員管理辦法征求意見稿
格式:pdf
大小:46KB
頁數:9P
4.6
醫療器械監督檢查員管理辦法征求意見稿 附件醫療器械監督檢查員管理辦法(征求意見稿)第 一章總則第一條為加強醫療器械監督檢查2員(以下簡 稱檢查員)的管理,做好醫療器械監督管理工作,依據醫療 器械監督管理條例等法規規章,制定本辦法。 第二條本辦法適用于依照醫療器械法規和相應質量管 理規范對醫療器械生產、經營或使用等環節開展檢查的相關 檢查員的管理。 第三條國家食品藥品監督管理總局(以下簡稱總局) 對檢查員實行分級管理,檢查員分為國家級、省級、地市級 和區縣級。 第四條總局負責制定全國檢查員隊伍建設的總體規 劃,制定發布檢查員管理制度并指導全國檢查員管理工作。 省級及以下食品藥品監督管理部門分別負責本轄區內 相應檢查員隊伍的建設規劃和管理。 第五條總局組織編寫統一的培訓教材,建立統一的考 試題庫,統一組織開展師資培訓。 第六條檢查員隊伍實行單位審核、教育培訓、資格考

醫療器械經營監督管理辦法(2014征求意見稿)
格式:pdf
大小:23KB
頁數:20P
4.7
醫療器械經營監督管理辦法 (征求意見稿) 第一章總則 第一條為加強醫療器械經營監督管理,規范醫療器械 市場秩序,保證醫療器械質量安全,根據《醫療器械監督管 理條例》,制定本辦法。 第二條在中華人民共和國境內從事醫療器械經營活動 及其監督管理,應當遵守本辦法。 第三條根據所經營醫療器械風險程度,對經營實施分 類管理。 第一類醫療器械的經營不需許可和備案;第二類醫療器 械的經營實行備案管理;第三類醫療器械的經營實行許可管 理。 第四條醫療器械經營企業應當按照《醫療器械經營質量 管理規范》開展經營活動,并承擔經營環節的質量管理責任。 《醫療器械經營質量管理規范》由國家食品藥品監督管 理總局制定。 第五條國家食品藥品監督管理總局負責全國醫療器械 經營監督管理工作。 地方各級食品藥品監督管理部門負責本行政區內醫療器 械經營的監督管理工作。 省級食品藥品監督管理部門負責指導和監督下級食

《醫療器械監督檢查員管理辦法》(征求意見稿)
格式:pdf
大小:12KB
頁數:9P
4.5
—2— 附件 醫療器械監督檢查員管理辦法 (征求意見稿) 第一章總則 第一條為加強醫療器械監督檢查2員(以下簡稱檢查 員)的管理,做好醫療器械監督管理工作,依據《醫療器械 監督管理條例》等法規規章,制定本辦法。 第二條本辦法適用于依照醫療器械法規和相應質量管 理規范對醫療器械生產、經營或使用等環節開展檢查的相關 檢查員的管理。 第三條國家食品藥品監督管理總局(以下簡稱總局)對檢 查員實行分級管理,檢查員分為國家級、省級、地市級和區縣級。 第四條總局負責制定全國檢查員隊伍建設的總體規 劃,制定發布檢查員管理制度并指導全國檢查員管理工作。 省級及以下食品藥品監督管理部門分別負責本轄區內相 應檢查員隊伍的建設規劃和管理。 第五條總局組織編寫統一的培訓教材,建立統一的考 試題庫,統一組織開展師資培訓。 第六條檢查員隊伍實行單位審核、教育培訓、資格考 試、考察聘用和綜合考評的

《安徽省醫療器械經營監督管理辦法實施細則》(征求意見稿)
格式:pdf
大小:248KB
頁數:28P
4.6
1 安徽省醫療器械經營監督管理辦法實施細則 (征求意見稿) 2015年9月30日 第一章總則 第一條為加強醫療器械經營監督管理,規范我省醫療器械經營秩序,根據 《醫療器械監督管理條例》(國務院令第650號)、《醫療器械經營監督管理 辦法》(國家食品藥品監督管理總局令第8號,以下簡稱《辦法》)、《醫療 器械經營質量管理規范》(國家食品藥品監督管理總局公告2014年第58號, 以下簡稱《規范》)和《醫療器械經營企業分類分級監督管理規定》(國食藥監 械〔2015〕158號)等,結合我省實際,制定本細則。 第二條在安徽省行政區域內從事醫療器械經營活動及其監督管理,應當遵 守本細則。 第三條按照醫療器械風險程度,對醫療器械經營實施分類管理;經營第一 類醫療器械不需許可和備案,經營第二類醫療器械實行備案管理,經營第三類醫 療器械實行許可管理。 第四條安徽省食
醫療器械不良事件監測管理辦法最新文檔

醫療器械管理制度
格式:pdf
大小:19KB
頁數:14P
4.4
'. 醫療器械使用前質量檢查制度 為了加強醫療器械的監督管理,保證產品的安全、有效,在醫療 器械使用前,嚴格遵循醫療器械使用前質量檢查制度。 一、醫院采購醫療器械,要根據《醫療器械監督管理條例》、《消 毒管理辦法》和《一次性使用無菌醫療器械監督管理辦法(暫行)》 的要求進行索證。凡證件不齊者,一律不予投入臨床使用。 二、醫療器械投入使用前,必須驗明產品合格證明和標簽標識, 建立真實完整的記錄,記錄應包括供貨單位、產品名稱、生產廠商、 生產許可證、注冊證號、規格型號、產品批號(編號)、生產日期(滅 菌日期)、有效期、購進數量、購進日期、驗收結論、驗收人簽名等。 三、根據采購計劃、進貨發票或送貨單,對產品名稱、生產廠 商、生產許可證、注冊證號、規格(型號)、批號(編號)、生產日期 (滅菌日期)、有效期、供貨單位、數量、日期等逐項核對、清點。 如有不相符或破損應及時做好記錄,嚴禁投入臨

醫療器械廠房巡查記錄表
格式:pdf
大小:41KB
頁數:3P
4.3
巡查時間:年月日 巡查 項目正常異常原因及處理情況 設備(干燥機附屬設施及雨棚、4臺 空調散熱器、) 完好 門窗、夾層百葉窗完好 消防設施完好 玻璃大廳完好 照明、滅蠅燈、壓差表、傳遞窗完好 設備、桌椅潔凈、完好、擺放有序 門窗 潔凈、完好(包括玻璃及 鎖子) 地面潔凈、無新增劃痕 空調控制開關(3臺)完好 臭氧發生器(3臺)潔凈、完好 線槽完好 電箱 潔凈、完好、停用時處于 關閉狀態 設備(純水機、空壓機)、照明 完好、不用時處于關閉狀 態 桌椅、檢查儀器、玻璃容器、潔具潔凈、擺放整齊 給排水閥門及管道完好 門窗完好 電箱、空開、傳遞窗潔凈、完好、不用時關閉 清洗池潔凈、完好 給排水閥門及管道潔凈、完好 容器、桌椅潔凈、擺放整體有序 發生器 潔凈、完好、不用時拔掉 插頭 雨具架、更鞋凳完好、潔凈、擺放整體 飲水機 潔凈、完

醫療器械行業咨詢合同
格式:pdf
大小:11KB
頁數:3P
4.4
醫療器械行業咨詢合同 ******有限公司(以下簡稱“委托方”)計劃開展醫療器械產品的研發和制造,特 委托**********(以下簡稱“受托方”),就“醫療器械企業開辦和產品注冊等”提供咨 詢服務,雙方就此簽署如下合同: 1委托內容 (1)對委托方公司現有情況進行調研; (2)對委托方公司未來規劃進行調研; (3)對委托方公司擬開發的產品進行調研和咨詢; (4)對委托方公司醫療器械企業開辦提供咨詢; (5)對委托方公司醫療器械產品注冊或備案提供咨詢; (6)對委托方公司醫療器械產品開發流程提供咨詢; (7)對委托方公司醫療器械行業法律法規提供培訓和咨詢; (8)委托方與受托方商議決定的其他咨詢內容。 2咨詢辦法和提供的文件 受托方根據上述項目規定的任務進行調研、培訓和咨詢;主要通過以下方 式提供服務: 1)通過當面的技術交流和指導,使委托方的公司未來規
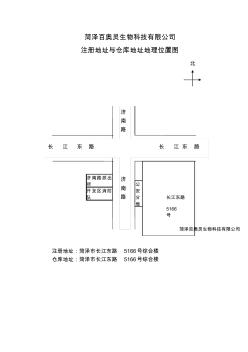
醫療器械地址平面圖
格式:pdf
大小:42KB
頁數:3P
4.6
菏澤百奧靈生物科技有限公司 注冊地址與倉庫地址地理位置圖 北 注冊地址:菏澤市長江東路5166號綜合樓 倉庫地址:菏澤市長江東路5166號綜合樓 濟 南 路 濟 南 路 菏澤百奧靈生物科技有限公司 長江東路 5166 號 長江東路長江東路 開發區消防 隊 濟南路派出 所公 安 分 局 菏澤百奧靈生物科技有限公司 經營場所平面布局圖 北 20m 12m4m4m 展示柜 營業區 8m辦公區 展示臺 經營場所面積:160㎡ 注冊地址:菏澤市長江東路5166號綜合樓 菏澤百奧靈生物科技有限公司 倉庫平面布局圖 北 7.5m 合格區 合格區 8m

醫療器械注冊細則號
格式:pdf
大小:228KB
頁數:25P
4.4
. 部分內容來源于網絡,有侵權請聯系刪除! 附件1 中華人民共和國醫療器械注冊證 (格式) 注冊證編號: 注冊人名稱 注冊人住所 生產地址 代理人名稱(進口醫療器械適用) 代理人住所(進口醫療器械適用) 產品名稱 型號、規格 結構及組成 適用范圍 附件產品技術要求 其他內容 備注 審批部門:批準日期:年月日 有效期至:年月日 (審批部門蓋章) . 部分內容來源于網絡,有侵權請聯系刪除! 附件2 中華人民共和國 醫療器械注冊變更文件 (格式) 注冊證編號: 產品名稱 變更內容 “***(原注冊內容或項目)”變更為“***(變更后的 內容)”。 備注 本文件與“”注冊證共同使用。 審批部門:批準日期:年月日 (審批部門蓋章) . 部分內容來源于網絡,有侵權請聯系刪除! 附件3 國家食品藥品監督管理總局 醫療器械臨床試驗批件 (格式) 批件號

醫療器械潔凈廠房
格式:pdf
大小:36KB
頁數:3P
4.7
關于醫療器械生產用潔凈廠房建設的要求 《體外診斷試劑生產實施細則(試行)》已實施近兩年,2011年將實施《無菌和植入 醫療器械生產質量體系管理規范》,在日常監管過程中,發現目前部分企業潔凈產房建設不 夠規范。為此,現提出潔凈廠房的建設要求如下: 一、目前涉及的標準和工作文件 1、yy0033-2000無菌醫療器具生產管理規范; 2、yy/t0567.1-2005醫療產品的無菌加工第1部分:通用要求; 3、yy/t0567.2-2005醫療產品的無菌加工第2部分過濾; 4、gb50457-2008醫藥工業潔凈廠房設計規范; 5、《體外診斷試劑生產實施細則(試行)》中附錄a; 6、《關于印發醫療器械生產質量管理規范無菌醫療器械實施細則和檢查評定標準(試 行)的通知》(國食藥監械[2009]835號); 7、《關于印發醫療器械生產質量管理規范植入性醫療

2015年2月最新發布關于征求醫療器械生產質量管理規范無菌醫療器械附錄
格式:pdf
大小:71KB
頁數:10P
4.6
inordertoensurestudeconsent,ntrunwithoutorgaanddisanormalteachingppearancestorenization.withouttordeport;rer,prheapprovalofrelevaotectingportoftheaccidenttoastudents'hentdealthygrowtpartments,mayorgawrittenreportintrih,ensuringthatnatinizestplicate,audeonal(prntstocorrectionalcentre,aparticipateioperty)isnotlost,
醫療器械不良事件監測管理辦法相關
文輯推薦
知識推薦
百科推薦

職位:消防施工團隊
擅長專業:土建 安裝 裝飾 市政 園林







