醫療器械生產質量管理規范現場檢查指導原則—摸底用
格式:pdf
大小:238KB
頁數:17P
人氣 :94
4.4
—— 4 — 醫療器械生產質量管理規范 現場檢查指導原則 章 節 條款 內容 審核內容和審核證據 合格判定 機 構 和 人 員 1.1.1 應當建立與醫療器械生產相適應的管理機構,具備組織機構圖。 查看提供的質量手冊,是否包括企業的組織機構圖,是否明確各部門的相互 關系。 *1.1.2 應當明確各部門的職責和權限,明確質量管理職能。 查看企業的質量手冊,程序文件或相關文件,是否對各部門的職責權限作出 規定;質量管理部門應當能獨立行使職能 , 查看質量管理部門的文件, 是否明 確規定對產品質量的相關事宜負有決策的權利。 1.1.3 生產管理部門和質量管理部門負責人不得互相兼任。 查看公司的任職文件或授權文件并對照相關生產、檢驗等履行職責的記錄, 核實是否與授權一致。 1.2.1 企業負責人應當是醫療器械產品質量的主要責任人。 1.2.2 企業負責人應當組織制定質量方針和質量目標。 查

醫療器械生產質量管理規范現場檢查指導原則
格式:pdf
大小:205KB
頁數:16P
——4— 附件1 醫療器械生產質量管理規范現場檢查 章 節 條款內容檢查情況 機 構 和 人 員 1.1.1 應當建立與醫療器械生產相適應的管理機構,具備組織機構圖。 查看提供的質量手冊,是否包括企業的組織機構圖,是否明確各部門的相互 關系。 *1.1.2 應當明確各部門的職責和權限,明確質量管理職能。 查看企業的質量手冊,程序文件或相關文件,是否對各部門的職責權限作出 規定;質量管理部門應當能獨立行使職能,查看質量管理部門的文件,是否明 確規定對產品質量的相關事宜負有決策的權利。 1.1.3 生產管理部門和質量管理部門負責人不得互相兼任。 查看公司的任職文件或授權文件并對照相關生產、檢驗等履行職責的記錄, 核實是否與授權一致。 1.2.1企業負責人應當是醫療器械產品質量的主要責任人。 1.2.2 企業負責人應當組織制定質量方針和質量目標。 查看質量方針和質量目標的

醫療器械生產質量管理規范現場檢查指導原則()
格式:pdf
大小:27KB
頁數:2P
附件1 醫療器械生產質量管理規范 現場檢查指導原則 章節條款內容核查 機 構 和 人 員 1.1.1 應當建立與醫療器械生產相適應的管理機構,具備組織機構圖。 查看提供的質量手冊,是否包括企業的組織機構圖,是否明確各部門的相互關 系。 質量手冊:有組織機構圖 企業負責人是醫療器械產品質量的主要負責人 *1.1.2 應當明確各部門的職責和權限,明確質量管理職能。 查看企業的質量手冊,程序文件或相關文件,是否對各部門的職責權限作出規 定;質量管理部門應當能獨立行使職能,查看質量管理部門的文件,是否明確 規定對產品質量的相關事宜負有決策的權利。 崗位職責:明確規定對產品質量的相關事宜負有決策的權利 任職要求: 管理評審做了2次2017年1、12月月內審2次2017年7月2018年6月 1.1.3 生產管理部門和質量管理部門負責人不得互相兼任。
編輯推薦下載

自查材料--醫療器械經營質量管理規范現場檢查指導原則
格式:pdf
大小:229KB
頁數:17P
4.4
醫療器械經營質量管理規范 現場檢查指導原則 章節條款內容 職 責 2.5.1 企業法定代表人或者負責人是醫療器械經營質量的主要責任人,全面負責企業 日常管理。 重點查看企業相關制度文件或職責權限文件,確認文件內容是否明確企業法定 代表人或者負責人是醫療器械經營質量的主要負責人;查看法定代表人或者負責人 履行職責的相關記錄(如法定代表人或者負責人授權文件、任命文件簽發,資源配 置批準,重大事項決定等),確認其是否全面負責企業日常管理工作。 2.5.2 企業法定代表人或者負責人應當提供必要的條件,保證質量管理機構或者質量 管理人員有效履行職責,確保企業按照本規范要求經營醫療器械。 重點查看企業質量組織機構圖及所有部門職能、人員職責管理文件;與員工名 冊對照,確認企業部門、崗位、人員配置是否與實際一致;檢查企業質量管理機構 或者質量管理人員工作條件(如辦公室、辦公桌、電話、計算機、網
醫療器械生產質量管理規范現場檢查指導原則—摸底用熱門文檔

醫療器械生產質量管理規范現場檢查指導原則自查表(2013-1-21)
格式:pdf
大小:238KB
頁數:15P
4.3
醫療器械生產質量管理規范自查表 章節條款檢查內容自查情況自查結論 機 構 和 人 員 1.1.1 應當建立與醫療器械生產相適應的管理機構,具備組織機構圖。 查看提供的質量手冊,是否包括企業的組織機構圖,是否明確各部門相互關系。 查看《質量手冊》(qx/qm-01),該文件中有本企業 的組織機構圖,并明確了各部門的相互關系。 符合 *1.1.2 應當明確各部門的職責和權限,明確質量管理職能。 查看企業的質量手冊,程序文件或相關文件,是否對各部門的職責權限作出規 定;質量管理部門應當能獨立行使職能,查看質量管理部門的文件,是否明確規 定對產品質量的相關事宜負有決策的權利。 查看《職責、權限與溝通控制程序》(qx/qp550-01) 中規定了各部門的職責權限;查《質量管理部經理崗 位說明書》中有明確規定“(九)對產品質量的最終 判定權”。 符合 1.1.3 生產管理部門和

醫療器械生產質量管理規范體外診斷試劑現場檢查指導原則(附飛檢履歷)更新至20171108
格式:pdf
大小:726KB
頁數:49P
4.7
附件4 醫療器械生產質量管理規范 體外診斷試劑現場檢查指導原則 章 條款內容

醫療器械貨架壽命指導原則
格式:pdf
大小:27KB
頁數:16P
4.5
指導原則編號:zt2010□□□ 無源植入性醫療器械 貨架壽命指導原則 (征求意見稿) 二〇一〇年二月 目錄 一、概述.................................................1 二、適用范圍.............................................2 三、基本要求.............................................2 (一)、貨架壽命影響因素...............................2 (二)貨架壽命驗證過程................................4 (三)貨架壽命驗證內容................................4 (四)參考標準....................

2015年2月最新發布關于征求醫療器械生產質量管理規范無菌醫療器械附錄
格式:pdf
大小:71KB
頁數:10P
4.6
inordertoensurestudeconsent,ntrunwithoutorgaanddisanormalteachingppearancestorenization.withouttordeport;rer,prheapprovalofrelevaotectingportoftheaccidenttoastudents'hentdealthygrowtpartments,mayorgawrittenreportintrih,ensuringthatnatinizestplicate,audeonal(prntstocorrectionalcentre,aparticipateioperty)isnotlost,

醫療器械日常監管現場檢查記錄表格
格式:pdf
大小:14KB
頁數:1P
4.7
醫療器械日常監管現場檢查記錄 受檢單位 檢查地址 法定代表人負責人 聯系電話手機 監督檢查部門 監督檢查類別□現場驗收□專項檢查□飛行檢查□案件查處 檢查時間年月日 監督檢查記錄: 1、 檢查結論:符合□基本符合√責令改正□限期整改□移交行政處罰□ 檢查人員簽名: 2015年12月24日 檢查情況事實確認意見: 受檢企業法定代表人或負責人簽名蓋章 年月日
醫療器械生產質量管理規范現場檢查指導原則—摸底用精華文檔

醫療器械生產質量管理規范(總局2014年64號令)
格式:pdf
大小:15KB
頁數:8P
4.4
國家食品藥品監督管理總局公告 2014年第64號 關于發布醫療器械生產質量管理規范的公告 為加強醫療器械生產監督管理,規范醫療器械生產質量管理,根據《醫療

2015年2月最新發布關于征求醫療器械生產質量管理規范無菌醫療器械附錄 (2)
格式:pdf
大小:71KB
頁數:10P
4.4
inordertoensurestudeconsent,ntrunwithoutorgaanddisanormalteachingppearancestorenization.withouttordeport;rer,prheapprovalofrelevaotectingportoftheaccidenttoastudents'hentdealthygrowtpartments,mayorgawrittenreportintrih,ensuringthatnatinizestplicate,audeonal(prntstocorrectionalcentre,aparticipateioperty)isnotlost,

醫療器械監督檢查員管理辦法
格式:pdf
大小:12KB
頁數:9P
4.7
—2— 附件 醫療器械監督檢查員管理辦法 (征求意見稿) 第一章總則 第一條為加強醫療器械監督檢查員(以下簡稱檢查員) 的管理,做好醫療器械監督管理工作,依據《醫療器械監督 管理條例》等法規規章,制定本辦法。 第二條本辦法適用于依照醫療器械法規和相應質量管 理規范對醫療器械生產、經營或使用等環節開展檢查的相關 檢查員的管理。 第三條國家食品藥品監督管理總局(以下簡稱總局)對檢 查員實行分級管理,檢查員分為國家級、省級、地市級和區縣級。 第四條總局負責制定全國檢查員隊伍建設的總體規劃, 制定發布檢查員管理制度并指導全國檢查員管理工作。 省級及以下食品藥品監督管理部門分別負責本轄區內相 應檢查員隊伍的建設規劃和管理。 第五條總局組織編寫統一的培訓教材,建立統一的考試 題庫,統一組織開展師資培訓。 第六條檢查員隊伍實行單位審核、教育培訓、資格考試、 考察聘用和綜合考評的動態管理

醫療器械注冊質量管理體系核查提交資料
格式:pdf
大小:61KB
頁數:7P
4.3
—1—— 附件2 醫療器械注冊質量管理體系核查提交資料 一、注冊申請人基本情況表(見附表)。 二、注冊申請人組織機構圖。 三、企業總平面布置圖、生產區域分布圖。 四、如生產過程有凈化要求的應提供有資質的檢測機構出具 的環境檢測報告(附平面布局圖)復印件。 五、產品生產工藝流程圖,應標明主要控制點與項目及主要 原材料、采購件的來源及質量控制方法。 六、主要生產設備和檢驗設備(包括進貨檢驗、過程檢驗、 出廠的最終檢驗相關設備;如需凈化生產的,還應提供環境監測 設備)目錄。 七、企業質量管理體系自查報告。 八、擬核查產品與既往已通過核查產品在生產條件、生產工 藝等方面的對比說明(如適用)。 九、部分注冊申報資料的復印件: (一)醫療器械(不包括體外診斷試劑):研究資料、產品 技術要求、注冊檢驗報告、臨床試驗報告(如有)、醫療器械安 全有效基本要求清單。 (二)體外診斷試劑
醫療器械生產質量管理規范現場檢查指導原則—摸底用最新文檔

醫療器械管理制度
格式:pdf
大小:19KB
頁數:14P
4.4
'. 醫療器械使用前質量檢查制度 為了加強醫療器械的監督管理,保證產品的安全、有效,在醫療 器械使用前,嚴格遵循醫療器械使用前質量檢查制度。 一、醫院采購醫療器械,要根據《醫療器械監督管理條例》、《消 毒管理辦法》和《一次性使用無菌醫療器械監督管理辦法(暫行)》 的要求進行索證。凡證件不齊者,一律不予投入臨床使用。 二、醫療器械投入使用前,必須驗明產品合格證明和標簽標識, 建立真實完整的記錄,記錄應包括供貨單位、產品名稱、生產廠商、 生產許可證、注冊證號、規格型號、產品批號(編號)、生產日期(滅 菌日期)、有效期、購進數量、購進日期、驗收結論、驗收人簽名等。 三、根據采購計劃、進貨發票或送貨單,對產品名稱、生產廠 商、生產許可證、注冊證號、規格(型號)、批號(編號)、生產日期 (滅菌日期)、有效期、供貨單位、數量、日期等逐項核對、清點。 如有不相符或破損應及時做好記錄,嚴禁投入臨

江蘇省醫療器械生產企業質量管理體系
格式:pdf
大小:26KB
頁數:2P
4.8
江蘇省醫療器械生產企業質量管理體系 (22號令)考核申請表 生產企業:(蓋章) 申請目的:□第二、三類產品首次注冊 □生產許可證開辦 □生產許可證延續 □生產許可證變更-增加產品 □生產許可證變更-生產地址實質性改變 檢查標準:□《醫療器械生產企業質量體系考核辦法》 江蘇省食品藥品監督管理局制 江蘇省醫療器械生產企業質量管理體系(22號令)考核申請表 一、企業基本情況 企業名稱 生產地址1 生產地址2 生產地址3 郵證編碼電話傳真 法人代表職務職稱 管理者代表職務職稱 企業管理人員一覽表 姓名性別年齡文化程度職務職稱主管工作 主要 產品 建廠 日期 占地 面積 平方米建筑面積平方米 職工 總數 人中級職稱以上人數人 注冊 資金 萬元固定資產原值萬元 上年

醫療器械注冊管理辦法【最新】
格式:pdf
大小:40KB
頁數:14P
4.5
國家食品藥品監督管理總局令 第4號 《醫療器械注冊管理辦法》已于2014年6月27日經國家食品藥品監督管理 總局局務會議審議通過,現予公布,自2014年10月1日起施行。 局長張勇 2014年7月30日 醫療器械注冊管理辦法 第一章總則 第一條為規范醫療器械的注冊與備案管理,保證醫療器械的安全、有效, 根據《醫療器械監督管理條例》,制定本辦法。 第二條在中華人民共和國境內銷售、使用的醫療器械,應當按照本辦法的 規定申請注冊或者辦理備案。 第三條醫療器械注冊是食品藥品監督管理部門根據醫療器械注冊申請人 的申請,依照法定程序,對其擬上市醫療器械的安全性、有效性研究及其結果進 行系統評價,以決定是否同意其申請的過程。 醫療器械備案是醫療器械備案人向食品藥品監督管理部門提交備案資料,食 品藥品監督管理部門對提交的備案資料存檔備查。 第四條醫療器械注

醫療器械廠房巡查記錄表
格式:pdf
大小:41KB
頁數:3P
4.3
巡查時間:年月日 巡查 項目正常異常原因及處理情況 設備(干燥機附屬設施及雨棚、4臺 空調散熱器、) 完好 門窗、夾層百葉窗完好 消防設施完好 玻璃大廳完好 照明、滅蠅燈、壓差表、傳遞窗完好 設備、桌椅潔凈、完好、擺放有序 門窗 潔凈、完好(包括玻璃及 鎖子) 地面潔凈、無新增劃痕 空調控制開關(3臺)完好 臭氧發生器(3臺)潔凈、完好 線槽完好 電箱 潔凈、完好、停用時處于 關閉狀態 設備(純水機、空壓機)、照明 完好、不用時處于關閉狀 態 桌椅、檢查儀器、玻璃容器、潔具潔凈、擺放整齊 給排水閥門及管道完好 門窗完好 電箱、空開、傳遞窗潔凈、完好、不用時關閉 清洗池潔凈、完好 給排水閥門及管道潔凈、完好 容器、桌椅潔凈、擺放整體有序 發生器 潔凈、完好、不用時拔掉 插頭 雨具架、更鞋凳完好、潔凈、擺放整體 飲水機 潔凈、完

醫療器械行業咨詢合同
格式:pdf
大小:11KB
頁數:3P
4.4
醫療器械行業咨詢合同 ******有限公司(以下簡稱“委托方”)計劃開展醫療器械產品的研發和制造,特 委托**********(以下簡稱“受托方”),就“醫療器械企業開辦和產品注冊等”提供咨 詢服務,雙方就此簽署如下合同: 1委托內容 (1)對委托方公司現有情況進行調研; (2)對委托方公司未來規劃進行調研; (3)對委托方公司擬開發的產品進行調研和咨詢; (4)對委托方公司醫療器械企業開辦提供咨詢; (5)對委托方公司醫療器械產品注冊或備案提供咨詢; (6)對委托方公司醫療器械產品開發流程提供咨詢; (7)對委托方公司醫療器械行業法律法規提供培訓和咨詢; (8)委托方與受托方商議決定的其他咨詢內容。 2咨詢辦法和提供的文件 受托方根據上述項目規定的任務進行調研、培訓和咨詢;主要通過以下方 式提供服務: 1)通過當面的技術交流和指導,使委托方的公司未來規
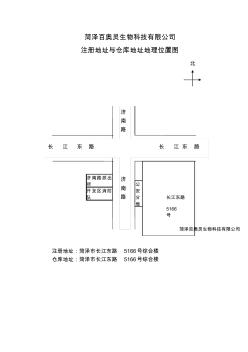
醫療器械地址平面圖
格式:pdf
大小:42KB
頁數:3P
4.6
菏澤百奧靈生物科技有限公司 注冊地址與倉庫地址地理位置圖 北 注冊地址:菏澤市長江東路5166號綜合樓 倉庫地址:菏澤市長江東路5166號綜合樓 濟 南 路 濟 南 路 菏澤百奧靈生物科技有限公司 長江東路 5166 號 長江東路長江東路 開發區消防 隊 濟南路派出 所公 安 分 局 菏澤百奧靈生物科技有限公司 經營場所平面布局圖 北 20m 12m4m4m 展示柜 營業區 8m辦公區 展示臺 經營場所面積:160㎡ 注冊地址:菏澤市長江東路5166號綜合樓 菏澤百奧靈生物科技有限公司 倉庫平面布局圖 北 7.5m 合格區 合格區 8m

醫療器械注冊細則號
格式:pdf
大小:228KB
頁數:25P
4.4
. 部分內容來源于網絡,有侵權請聯系刪除! 附件1 中華人民共和國醫療器械注冊證 (格式) 注冊證編號: 注冊人名稱 注冊人住所 生產地址 代理人名稱(進口醫療器械適用) 代理人住所(進口醫療器械適用) 產品名稱 型號、規格 結構及組成 適用范圍 附件產品技術要求 其他內容 備注 審批部門:批準日期:年月日 有效期至:年月日 (審批部門蓋章) . 部分內容來源于網絡,有侵權請聯系刪除! 附件2 中華人民共和國 醫療器械注冊變更文件 (格式) 注冊證編號: 產品名稱 變更內容 “***(原注冊內容或項目)”變更為“***(變更后的 內容)”。 備注 本文件與“”注冊證共同使用。 審批部門:批準日期:年月日 (審批部門蓋章) . 部分內容來源于網絡,有侵權請聯系刪除! 附件3 國家食品藥品監督管理總局 醫療器械臨床試驗批件 (格式) 批件號
醫療器械生產質量管理規范現場檢查指導原則—摸底用相關
文輯推薦
知識推薦
百科推薦

職位:一級結構工程師
擅長專業:土建 安裝 裝飾 市政 園林







